這是 KDIGO (The Kidney Disease: Improving Global Outcomes,一個致力於制定以實證醫學為基礎的腎臟病臨床指引的國際組織),於 2021出版的腎絲球疾病治療指引 ( Clinical Practice Guideline for the Management of Glomerular Diseases),因為太重要了,所以我們將讀書摘要與所有的人分享。
全文連結於此 (link),雖然我們盡力維持內容的正確性,若閱讀有疑義時還請以原文為正解。我們將為每章建立一個單元,各章節連結如下,我們也會建立相關的臨床病例、病理切片及文獻整理,若對您有幫助,也希望給我們一些回饋。
Chap 03 : 膜性腎絲球病變 (Membranous nephropathy)
♠ 這是林泰宇醫師的詳細版本,一併呈現 KDIGO 工作小組的建議
粗體:治療指引;♥ 指引細項;♦ 內文摘要;♣ 附圖說明
3.1 診斷
♦ 本章節提供18歲以上成人之膜性腎絲球病變 (Membranous nephropathy, MN)治療建議。兒童族群之MN資料非常有限,相關之處置建議放在治療要點 3.4.4
治療要點 3.1.1:在有腎病症候群 (nephrotic syndrome) 及 anti-PLA2R 抗體陽性的病人,不需以腎臟切片來確認 MN 的診斷
♦ 對於那些臨床表現符合的病人,確認MN的診斷對指引處置及治療非常關鍵。腎臟切片通常是診斷腎絲球疾病 (glomerular disease) 的黃金標準 (gold standard);然而,對於MN,anti-PLA2R抗體是高度準確性之生物指標 (biomarker),且沒有腎臟切片相關之風險,包括組織不足而無法做出有結論的診斷、疼痛、及出血。
♦ 因此,對於anti-PLA2R抗體陽性病人,只在另有診斷 MN 以外的目的才需要做腎臟切片。
♦ 目前的證據還不足以支持用 anti-THSD7A 抗體作為取代腎臟切片的 MN 診斷性生物指標。
♦ 在一篇 9 份研究的統合分析 (Meta-analysis) 中,包含 710 個 MN 病人及 1502 個對照組,以 anti-PLA2R 抗體陽性作為 MN 診斷的敏感性 (sensitivity) 為 0.78,特異性 (specificity) 為 0.99。
♦ 近期一篇單一中心研究 (single-center study) 確認了其高準確度,敏感性為 0.64和特異性為 0.99,特異性之95% 信賴區間 ( confidence interval,IC) 為0.96~1.0,與腎臟切片的診斷相似。
♦ 另一篇研究額外的腎臟切片在診斷 MN 的價值,收錄 97 位 anti-PLA2R抗體陽性且無證據有續發性 MN 致因的病患,做了腎臟切片後所有初步診斷都是 MN。在 60 位 eGFR>60 ml/min/1.73m2 的病人只有發現 2 位分別合併有糖尿病腎病變 (diabetic nephropathy) 或局部節段性腎絲球硬化症 (FSGS),這些發規不影響病人照顧或治療。另外 37 位 eGFR<60 ml/min/1.73m2 病患中有 5 位合併其他發現,包含 1 位急性間質性腎炎 (acute interstitial nephritis)、1 位糖尿病腎病變 (diabetic nephropathy)、1位急性腎小管壞死 (acute tubular necrosis)、2 位局部節段性腎絲球硬化症 (FSGS) 且其中一位有細胞新月狀 (cellular crescents)。雖然研究沒有提到、但是這些資訊有可能影響會治療。
♦ 最近一項研究結論強調在 anti-PLA2R抗體陽性且 eGFR 正常之病患,腎臟切片並不會改變原發性 MN 之診斷。
♦ 更多 anti-PLA2R 抗體分析方法之細節 ( Fig 27),以及何時該在 anti-PLA2R抗體陽性病患考慮執行腎臟切片 (Fig 28) 如以下說明。
♦ 對於 anti-PLA2R抗體陰性之病人,應安排腎臟切片且要染 PLA2R抗原,這或許會揭示 anti-PLA2R 抗體相關之 MN。會發生這些狀況是這些病人可能因為血清效價太低,導致血清酵素免疫吸附法 ( enzyme linked immunosorbent assay,ELISA) 和免疫螢光分析法 ( Immunofluorescence test) 出現偽陰性。
♦ 此外,在早期之 MN 有可能尚無抗體,被腎臟捕捉 (capture ),在長期追蹤後才變成可偵測。
Fig 27 在已知 anti-PLA2R 相關之 MN 病人,使用及判讀 anti-PLAR2 抗體測定的指引
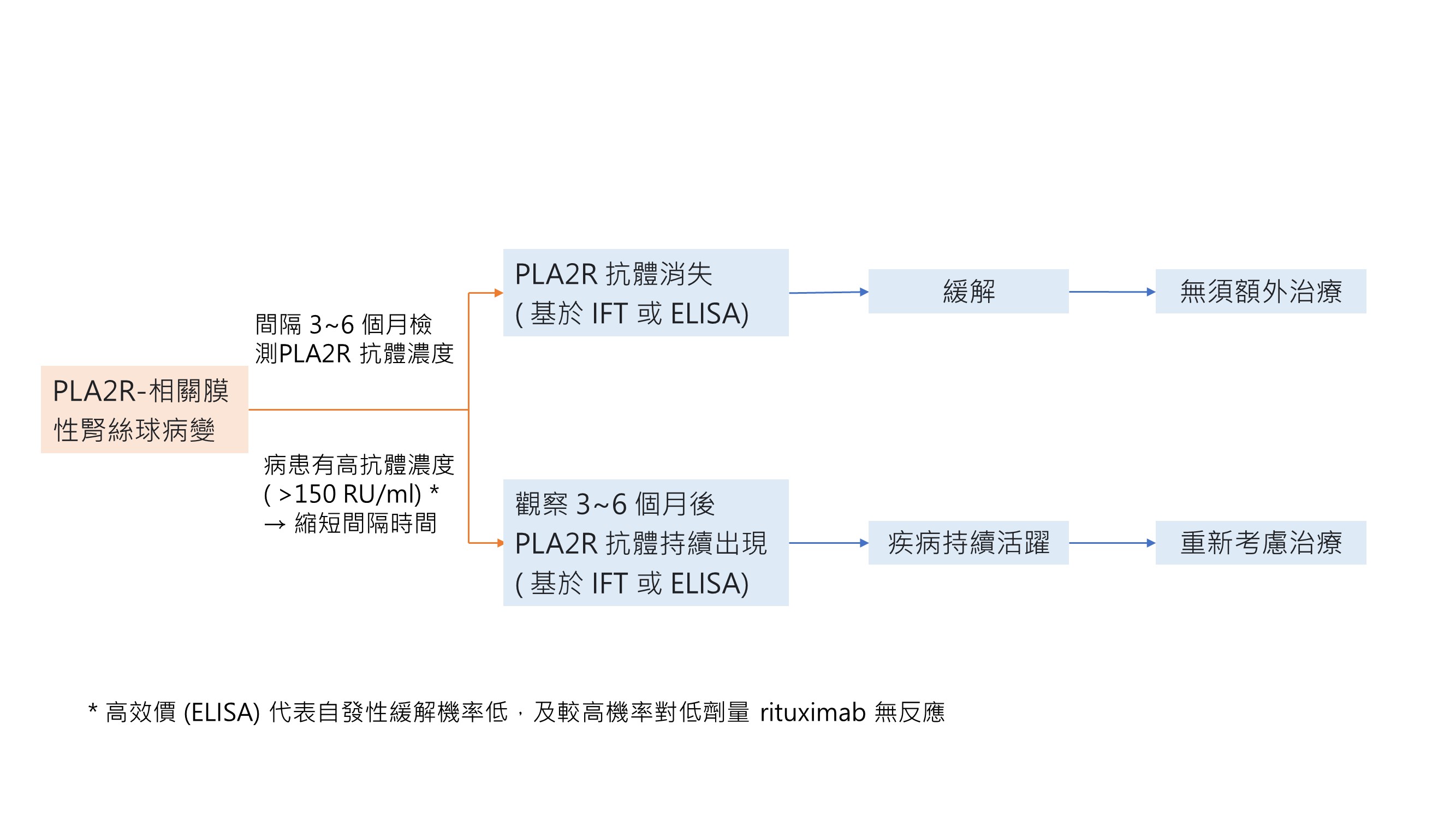
Fig 28: 在 anti-PLA2R 抗體陽性之病人何時須考慮做腎臟切片
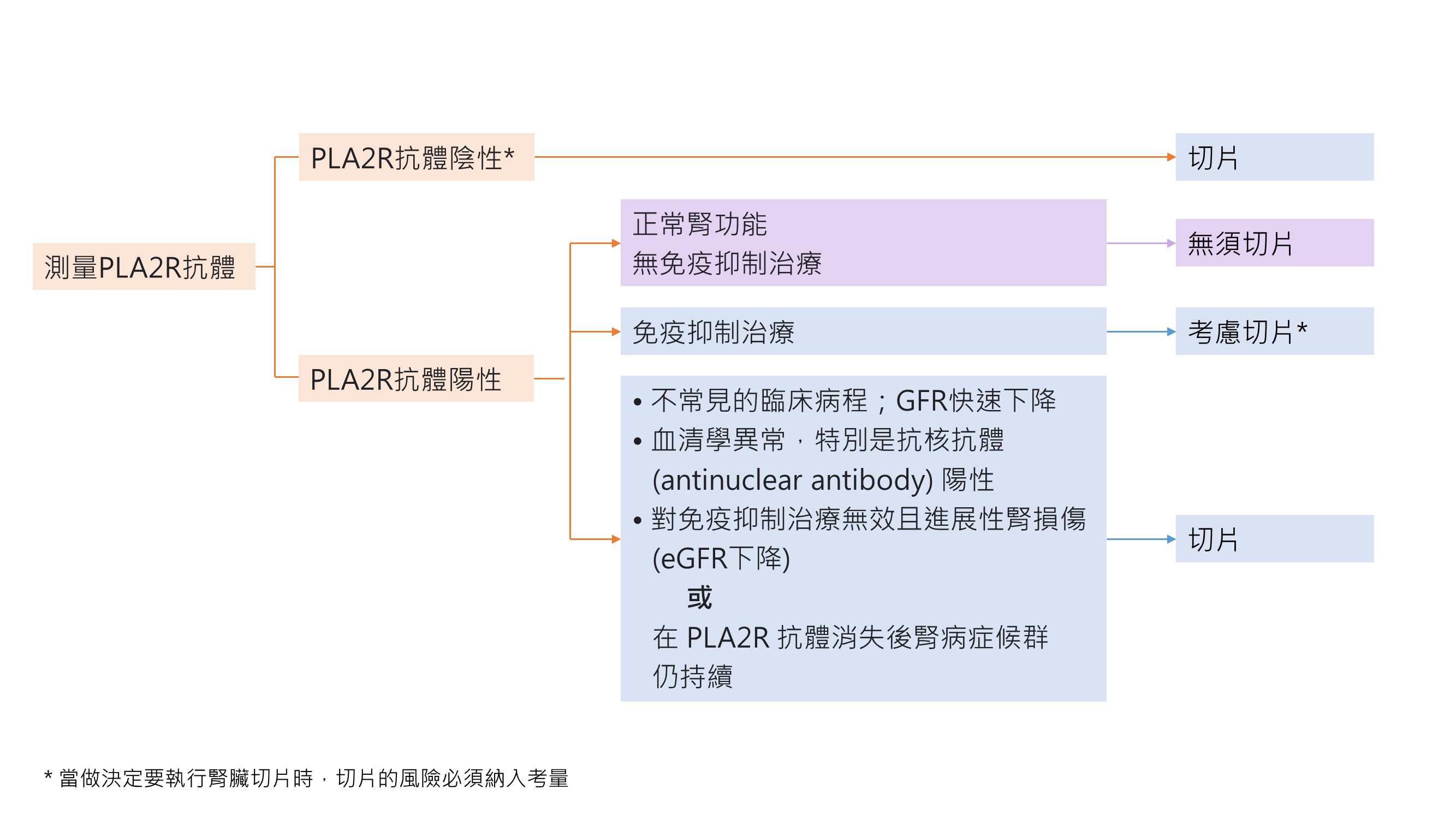
* 當做決定要執行腎臟切片時,切片的風險必須納入考量。此決定必須基於病患和醫師的選擇 ( preference)。
♣ 目前腎臟切片的決定可能會在不久後有所修訂,隨著分子診斷 ( molecular diagnostic) 的發展,更加個人化的醫療將更能預測疾病結果 ( outcome)。
治療要點 3.1.2:MN病患必須評估相關疾病,不論 anti-PLA2R 抗體和/或 anti-THSD7A抗體為陰性或陽性 (Fig 29)
Fig 29 : 評估MN病患相關疾病
♥ 篩檢惡性腫瘤* (對應合適之族群及年紀)
♥ 腎臟超音波
♥ HBV、HCV、HIV和梅毒檢查 ( 按適應症)
♥ 胸腔X光 ( 類肉瘤病,sarcoidosis)
♥ 藥物使用病史 (NSAID、金、penicillamine)
♥ 抗核抗體 (antinuclear antibodies)
♥ 完整病史詢問 (系統性疾病、甲狀腺疾病等) 和身體檢查 (皮膚、關節)
* 因各國而異,癌症篩檢之發現不會太高,尤其在年輕病人。許多醫療中心會安排胸部 X 光或電腦斷層檢查 (CT),排除鐵不足 ( iron deficiency),及要求病人加入國家乳癌及大腸癌篩檢計劃;成人男性 > 50~60 歲檢測攝護腺特定抗原(Prostate-Specific Antigen,PSA)
3.2 預後
治療要點 3.2.1:在MN病人,用臨床和實驗室標準 (criteria) 去評估腎臟功能逐漸損失的風險 (Fig 30)
Fig 30:評估腎臟功能損失速度風險的臨床標準
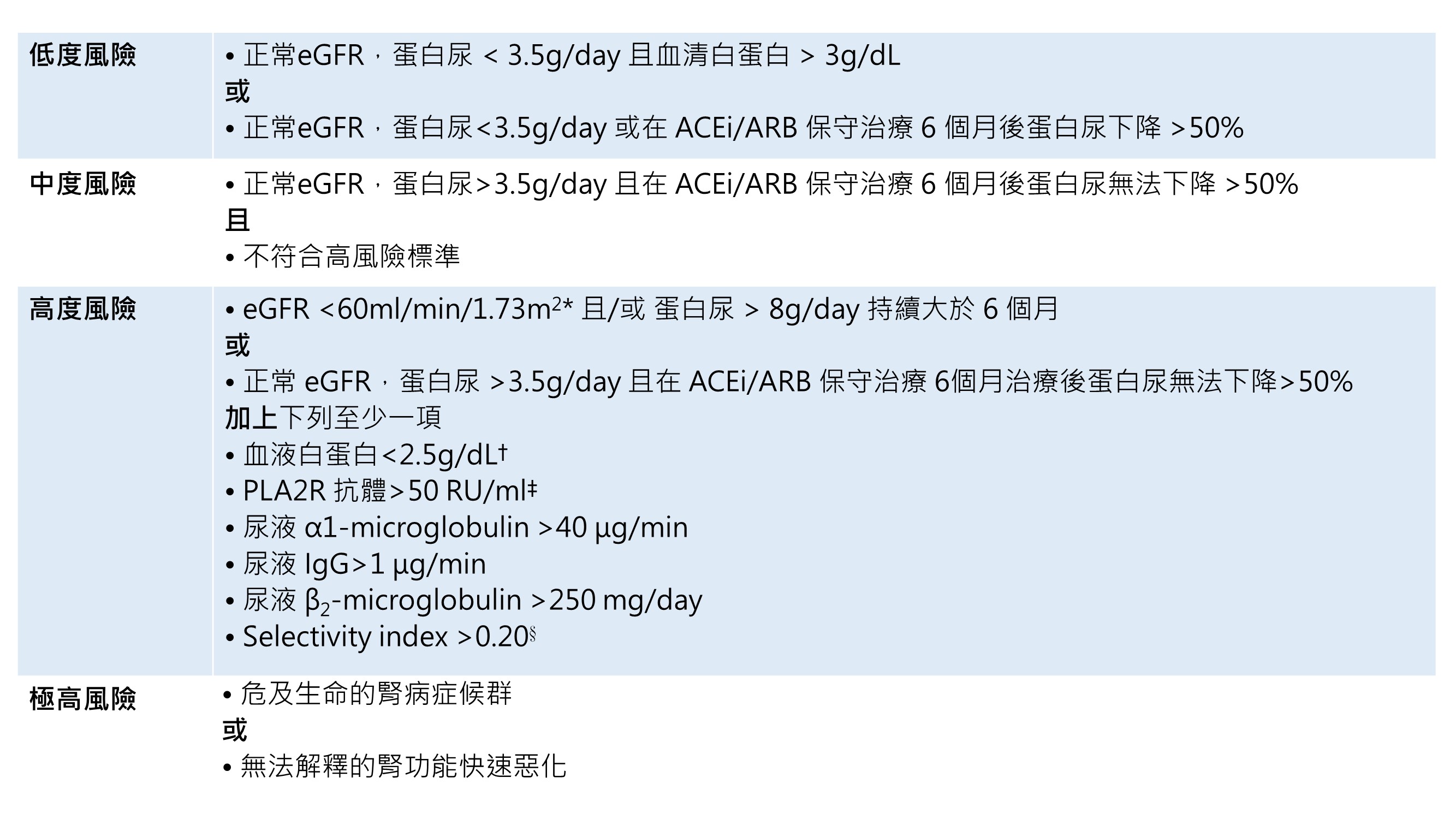
♣ eGFR 及 PCR 於例行臨床照護中使用,其他生物標記不一定在所有醫療中心都可取得,這張表格提供有用生物指摽的概述
♣ 大多研究使用血清肌酸酐 (serum Cr,SCr) 指引治療,SCr > 1.5mg/dL 常用於定義腎功能不全 ( renal insufficiency )。在年輕成人 eGFR 60 ml/min/1.73m2定義為腎功能不全。很重要的,須瞭解 eGFR 隨著年紀而下降,SCr 1.5mg/dL 所反映的是在 60 歲男性 eGFR 為 50 ml/min/1.73m2 在 60 歲女性則是 37 ml/min/1.73m2。因此,用 eGFR 做風險評估時,需將年紀列入考量
† 白蛋白需用 BCP 或免疫測定法 ( immunometric assay) 測量
‡ 閾值 ( cutoff value) 尚未確認。Anti-PLA2R抗體應每隔3~6個月測量,初始抗體效價高的病患應縮短間隔時間。Anti-PLA2R抗體在追蹤時的改變應列入風險評估。Anti-PLA2R抗體的消失先於臨床上的緩解,此時避免額外的治療
§選擇性指標 (Selectivity index) 的計算為 IgG清除率(clearance )/白蛋白清除率
♦ 因為自發性緩解在 MN相對常見,而免疫抑制治療有其副作用,在決定是否需要和何時開始免疫治療前,須要先完成腎臟功能逐漸損失的風險評估。
♦ Fig 30 依臨床標準把病人分類為低、中、高、非常高的腎臟功能損失風險。
♦ 評估 MN 的風險有下列說明以避免誤解 ( caveat)。
♦ 在大部分病人,使用最大劑量的抗蛋白尿治療 6 個月來等待疾病自發性緩解是很合理的。高程度的蛋白尿、anti-PLA2R抗體效價,或低分子蛋白尿 (low-molecular weight proteinuria) 的病人必須早於 6 個月就該重新評估。
♦ 腎功能持續惡化或是治療無效的嚴重腎病症候群病人,可能需要考慮立即給予免疫抑制治療,因為這些病患的 eGFR 有 84% 會在 24 個月內下降 20%。
♦ 文獻研究指出,蛋白尿 > 4g/day 的病人在 6 個月保守治療後有 45% 的機會自發性緩解,蛋白尿 > 8g/day 持續大於 6 個月者有 34% 的機會自發性緩解,嚴重低分子蛋白尿的病患有 25~30% 的機會,anti-PLA2R抗體效價在前 1/3 位數的病患有 17%,anti-PLA2R 抗體效價 >275 RU/ml 的病人有 20% 的機會 ( 個人溝通意見,personal communication)。
♦ 目前尚未有模型結合所有的臨床考量,但是我們建議考慮風險時要結合各項要素 ( 如., 嚴重蛋白尿而抗體效價低的病患,判斷上和嚴重蛋白尿但抗體效價高的病人會不一樣) 。
♦ 更重要的是,因為疾病本身的自然病程,以上提及的任一因子之變化皆應列入考量。
3.3 治療
治療要點 3.3.1:治療原發性 MN 的考量:
♥ 所有原發性 MN 且合併蛋白尿病人應接受合適的支持性療法
♥ 免疫抑制治療限制用於考量有腎臟逐漸損傷之風險的病人 (Fig 31)
Fig 31 : 基於風險之 MN 治療
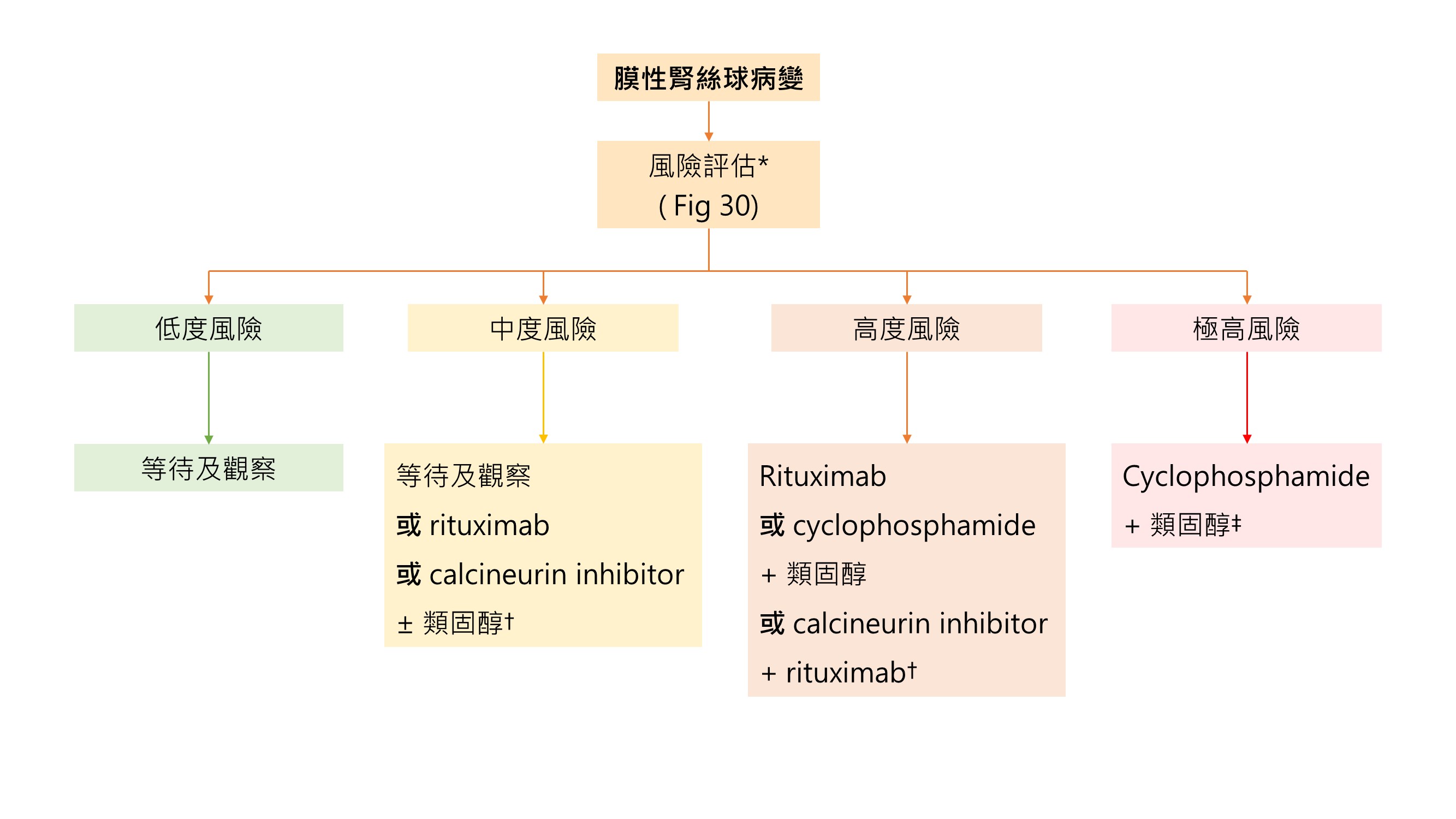
* 詳細風險評估之敘述請見治療要點 3.2.1 及 Fig 30
† Calcineurin inhibitor (CNI) 單一藥物治療效果較差,以 CNI 治療 6~12 個月後快速停藥有高復發率。不過,在 eGFR 正常及中等風險的病人仍可考慮使用,因為許多這樣的病人會自發性緩解。CNI 可以減少蛋白尿持續時間。對於高風險病人使用CNI 6 個月後建議加用 rituximab,anti-PLA2R 抗體在 CNI 治療後消失的病患除外
‡ 目前以標準劑量的 rituximab 預防腎衰竭之證據不足。如果 eGFR < 50 ml/min/1.73m2則 cyclophosphamide 劑量需減半。如果病患無法忍受或不能再使用 cyclophosphamide,則可以考慮rituximab
治療要點 3.3.2:對於蛋白尿 < 3.5g/d 且血清白蛋白 >3g/dL (BCP或免疫測定法)且 eGFR >60 ml/min/1.73m2的 MN 病人,不需要免疫抑制治療
♦ MN 病人如果是正常 eGFR 且蛋白尿未達腎病症候群範圍 ( 非腎病蛋白尿) 通常預後很好。
♦ 這些病人血栓栓塞併發症風險低而且症狀表現較輕微 (如., 水腫),所以能以保守治療處理 (Chap 1)。
♦ MN 病人有正常 eGFR 及非腎病蛋白尿時通常血清白蛋白 > 3g/dL,如果 < 3g/dL則需要排除其他造成低白蛋白的病因。
♦ 目前尚未有隨機臨床試驗 (RCT) 去比較 MN 及非腎病蛋白尿的病人接受或不接受免疫抑制治療之預後是否不同。
♦ 然而,臨床經驗以及世代研究 (cohort) 皆顯示 MN 且有持續非腎病蛋白尿的病人有良好的腎臟預後,儘管沒有接受免疫抑制治療。所以免疫抑制治療只會增添風險而沒有潛在的益處。
♦ 在追蹤時,可輕易地藉由腎病症候群之發展或eGFR下降來確認疾病之進展。
♦ 初始表現出高的 anti-PLA2R抗體效價與腎病症候群發展的風險相關聯。
治療要點 3.3.3:對於有腎病症候群但正常 eGFR 之 MN 病人不需疫抑制治療,除非有至少一種疾病惡化風險因子出現或是出現嚴重的腎病症候群併發症 (如., 急性腎損傷、感染、血栓栓塞事件)
♦ 許多原發性 MN 且有腎病症候群的病人會自發性緩解。目前仍未有臨床隨機試驗比較 MN 且無風險因子之病人接受免疫抑制治療與否之預後。然而,在其他隨機臨床試驗或是世代研究中,MN且至少有一種風險因子病患仍然有良好預後。這些研究顯示大約 40% 或更多病人會有自發性緩解。
♦ 如果沒有風險因子而且沒有腎病症候群的併發症出現,免疫抑制治療會增加傷害但只有些微助益。
♦ 將 MN 病患分類成低度、中度、高度及極高度腎臟逐漸喪失功能的風險,更能有效選擇出哪些病患比較可能會自發性緩解。
建議 3.3.1:對於至少有一種疾病進展風險因子之 MN 病患,我們建議依照估計之風險選擇治療 ( Fig 30 及 Fig 31 ),使用 6 個月 rituximab 或 cyclophosphamide與交替隔月之類固醇,或是以 CNI 為基礎之治療 ≧ 6 個月。(1B)
♦ 此建議較著重於在高風險病人預防腎衰竭進展,減少腎病症候群之風險與併發症,相對較不在意免疫抑制治療法的副作用與不便。治療選擇應依據病人特性,藥物可得性,藥物療效,病人、醫師、與社會的選擇,保險給付政策,及各別藥物的特定副作用去做選擇。
♦ 基於風險評估的治療流程如 Fig 31
♦ 常用治療處方詳如 Fig 32
Fig 32 : 常用 MN 治療處方

♣ Mycophenolate mofetil將不被討論,KDIGO 2012 治療指引反對使用 MMF 做為 MN單一藥物治療,目前仍維持這項決定而且有 1 RCT 結果支持,在這研究裡 36 位病患接受 MMF 單一藥物治療 12 個月後沒有增加緩減比例 ( 37% vs. 41% ),而且 MMF 併用類固醇比較有效。
♣ 有些小型 RCT 比較 MMF 加類固醇和烷化劑 ( alkylating agent) 或 CNI 的治療效果,這些實驗都只有較短的追蹤時間,結果在緩解比例上是相似的。
♣ 一篇研究以過往的控則組去比較 MMF 和 cyclophosphamide 發現有相似的緩解率,但是在 24 個月內追蹤的復發率在 MMF 組別顯著上升。
♣ 一篇更詳細評估的研究顯示使用 MMF 較難達成免疫緩解。MMF 使用的劑量可能是最相關的變數:狼瘡性腎炎( LN) 研究使用較高劑量 (3g vs. 2g),在類固醇有效之腎疾症候群 (SSNS) 病人有較高藥物濃度者有較低復發比例。
註:Prednisone 和 prednisolone 是相等的,使用同樣的劑量,依照著實驗來源的國家所不同都曾在 RCTs使用過。後面提到所有的 ” prednisone” 可代表 prednisone 或 prednisolone,所有提到的 ”類固醇” ( glucocorticoids) 意指 prednisone 或 prednisolone,除非有特別說明。
‡目前的研究曾使用靜脈注射 cyclophosphamide,這些研究包括 eGFR 正常的病患。目前尚未有RCT去評估靜脈注射 cyclophosphamide對於腎臟終點 ( endpoint ) 的效用。早期的 RTCs 在 eGFR 惡化的病人使用脈注射 cyclophosphamide 是負面的 ( negative) 。因此對於正常eGFR的病人但想要使用最低的累積劑者 ( 之前曾使用過,病人想耍懷孕 ),或是口服劑型無法取得的國家,或許可以考慮靜脈注射cyclophosphamide。
* 如果病人腎病症候群持續,有穩定 eGFR,尤其是 anti-PLA2R 抗體仍然陽性時,考慮在 6 個月後重複使用
† Cyclosporine 和 tacrolimus 通常會合併 prednisone 10 mg/d使用。4 個月後如果無效就停止;12 個月後考慮漸減藥物到低劑量。只有少數臨床試驗比較 CNI 藥物的劑量和治療時間。一篇研究比較 6 個月和 24 個月的 tacrolimus 及 prednisone 治療,緩解率在 6 個月後相似 (18/20 vs, 18/22),但是 24 個月後持續緩解在 6 個月的治療組只有 9/18,但在 24 個月的治療組為 18/18。一篇統合分析確認了 CNI的高緩解率和高復發率。這些發現可以跟病人在決定治療期之長短時討論。
重要資訊 (key information)
益處與損害之平衡 (Balance of benefits and harms)
♦ 很多 MN 合併腎病症候群的病人會自發性緩解。任何免疫抑制藥物都有其風險,因此,當病人有足夠的抱怨和/或有腎病症候群之風險 (如水腫、感染、血栓事件、腎衰竭惡化),以及自發性緩解可能性低時,才有理由 ( justifiable) 使用免疫抑制治療。
♦ 隨機臨床試驗和世代研究皆顯示 rituximab 和 CNI 能增加完全或部分緩解比例。這些藥物的效益及副作用的持性此起 cyclophosphamide 來說更適合用於 MN 且維持腎功能的病人之初始治療。CNI 的高復發率是需要擔憂的原因,因此 CNI 單一藥物治療只有在疾病進展中等風險的病患可以合理使用。
♦ 烷化劑 (Alkylating agents) 不但能夠增加緩解率,更重要的是也能大幅降低腎衰竭風險。烷化劑是有毒性之藥物,常常伴隨嚴重的短期及長期副作用。雖然證據等級是中等品質 (moderate quality),考量其毒性特性,基於 cyclophosphamide 的免疫抑制治療應該只限制用於高風險病人。
♦ Cyclophosphamide 優於 chlorambucil,雖然證據並不充足,但是一篇臨床隨機試驗和多個世代研究顯示 cyclophosphamide 副作用較少。在 CKD 病人較常需調整 chlorambucil的 劑量和治療時程,或許可以解釋為何其緩解率較低。
證據品質 ( Quality of evidence)
♦ 由證據審查組 ( evidence review team , ERT) 評估隨機臨床試驗的證據品質。
♦ 比較口服烷化劑和安慰劑/不使用烷化劑 ( no treatment) 或類固醇的RCTs之證據等級被認為是中等 (moderate),因為有嚴重的偏差 (bias) 的風險與缺乏遮盲 (blinding)。
♦ 烷化劑是唯一在試驗曾評估關鍵結果 ( critical outcome) 如總死亡率 (all-cause mortality) 和腎衰竭的藥物。
♦ Rituximab 或 CNIs 的隨機臨床試驗僅評估緩解率和副作用。
♦ Evaluate Rituximab Treatment for Idiopathic Membranous Nephropathy (GEMRITUX) RCT 試驗 rituximab 加上保守治療和只用保守治療的比較,The Membranous Nephropathy Trial Of Rituximab (MENTOR) 比較 rituximab 和cyclosporine。就效用的結果 (outcome) 如完全/或部分緩解,其證據等級各是低和中等,因為有嚴重的不精確。其他結果 (outcome) 如感染也是低品質的證據,因為嚴重的不精確 ( 寬的信賴區間代表效果的不確定性 )。
♦ 臨床試驗中以CNIs 比較安慰劑,不使用 CNI,類固醇,烷化劑治療效果的證據等級都是很低 (very low),因為不精確,信賴區間寬,而且關鍵結果的追蹤時間不夠長 (總死亡率、腎衰竭)。
♦ 那些追蹤時間夠久到達成完全緩解的試驗,都有嚴重的實驗限制 (limitation) 以及高偏差 (bias) 風險的嚴重問題,包括像是實驗人員和受試者缺乏遮盲 (blinding),結果分析人員不清楚是否有遮盲、受試者數目不足,以及收錄只有摘要的文章。
♦ 對於罕見疾病、尤其是有嚴重、客觀的臨床結果如死亡率、腎衰竭,證據不應該只局限於隨機臨床試驗的資料。工作小組因此使用非隨機臨床試驗 (non-RCTs) 和世代研究來做為部份的證據基礎。
♦ 工作小組強調使用風險評估的需要,以便能相當精確地辨識高風險病人 ( 治療要點 3.2.1)。
♦ 基於 RCTs 及世代研究,有強度 (strong) 等級證據顯示烷化劑可降低腎衰竭風險。有中度 (moderate) 品質的證據顯示烷化劑在有侷限性的治療策略 (restrictive treatment strategy),及在腎功能惡化的病人是有效的。
♦ 無證據顯示 rituximab 或 CNIs 可以降低腎衰竭風險。
♦ 中度品質的證據顯示 rituximab 或 CNIs 可以增加完全或部分緩解率。
♦ 在腎病症候群病人的試驗裡,完全緩解 (中度品質) 和部分緩解 (低度品質) 可以做為代理臨床試驗終點 ( surrogate endpoint)。
♦ 中度品質的證據顯示烷化劑比 rituximab 或 CNIs 有較頻繁且較嚴重的副作用。
♦ CNI 的使用有高復發率。中度品質的證據顯示使用 rituximab 後的緩解較 CNIs 為持續。
價值與偏好(values and preferences)
♦ 免疫抑制治療有其副作用。對於那些有較好臨床病程 ( 治療要點 3.2.1)、或是比較擔心免疫抑制治療副作用的病患會傾向拒絕這些治療。相反地,那些有嚴重腎病症候群症狀或是併發症 (血栓栓塞事件、感染、急性腎損傷) 的病人比較願意接受治療。
♦ Rituximab 或 CNIs 相對 cyclophosphamide 有較少且較不嚴重的副作用,因此大多數醫師及病人較顧意選擇 rituximab 或 CNIs 作為起始治療。
♦ 腎衰竭是 MN 最常見且最嚴重的併發症,雖然病患可以經由腎臟替代療法 (kidney replacement therapy) 存活,但是此治療有很高的發病率和死亡率。而且,大部分腎衰竭病人會想接受腎臟移植,但是這會需要終身服用免疫抑制藥物。
♦ 在工作小組的判斷中,大部分充分被告知有 (很高風險) 腎衰竭的病患都會接受cyclophosphamide 治療而非只是保守治療。
♦ 治療的起始時間,藥物的種類,以及治療時程需要倚賴風險評估,病人特性,病人與醫師的偏好,保險給付政策,以及社會的觀點 ( 價格和藥物可得性)。
資源利用和成本 ( Resource use and costs)
♦ 免疫抑制治療法需要很高花費,包括治療本身,監控、和處理副作用。
♦ 腎臟替代治併隨低生活品質、較高花費、承擔和免疫抑制治療法類似甚至更高的副作用。
♦ 免疫抑制療法能夠預防腎功能惡化以及腎衰竭,因此這項建議從醫療系統的觀點而言是具成本效益 (Cost-efficacy)的。
♦ 成本效益在可預期會順利恢復的病人上較難顯現。在中等風險病人,治療的副作用會導致成本增加,因此,選擇副作用較小的藥物會比較有成本效益。
♦ 藥物的可得性在每個國家和地區都不相同。
實行的考量 ( Considerations for implementation)
♦ MN病人有腎病症候群症狀,併發症,或是腎衰竭風險,有可能受益於免疫抑制治療。這項建議對所有性別或種族皆適用。
理論基礎 (Rationale)
♦ 這項建議取代了 2012 KDIGO 的建議,雖然承認烷化劑在預防腎衰竭的已知效用,現今這項建議更著重在嚴重的短期及長期副作用。醫師和病人也特別會對致癌的長期風險有所畏懼,因此,會選擇有效的替代治療。
♦ Rituximab 或 CNIs 為基礎的治療現已引為合適的替代性選擇。儘管缺乏rituximab 或 CNIs對於預防腎衰竭的直接證據,工作小組著重在研究所顯示這兩些藥物有高緩解率,和讚賞其持續的緩解時間及良好腎臟預後。
♦ 對於 eGFR 下降之病人,只有烷化劑證實是有效的。
治療要點 3.3.4:對於 MN 病患,在治療開始 6 個月後持續監測 anti-PLA2R 抗體效價有助於評估治療反應,也能用於指引治療之調整 (Fig 33 )
Fig 33:MN在接受治療後的免疫監測
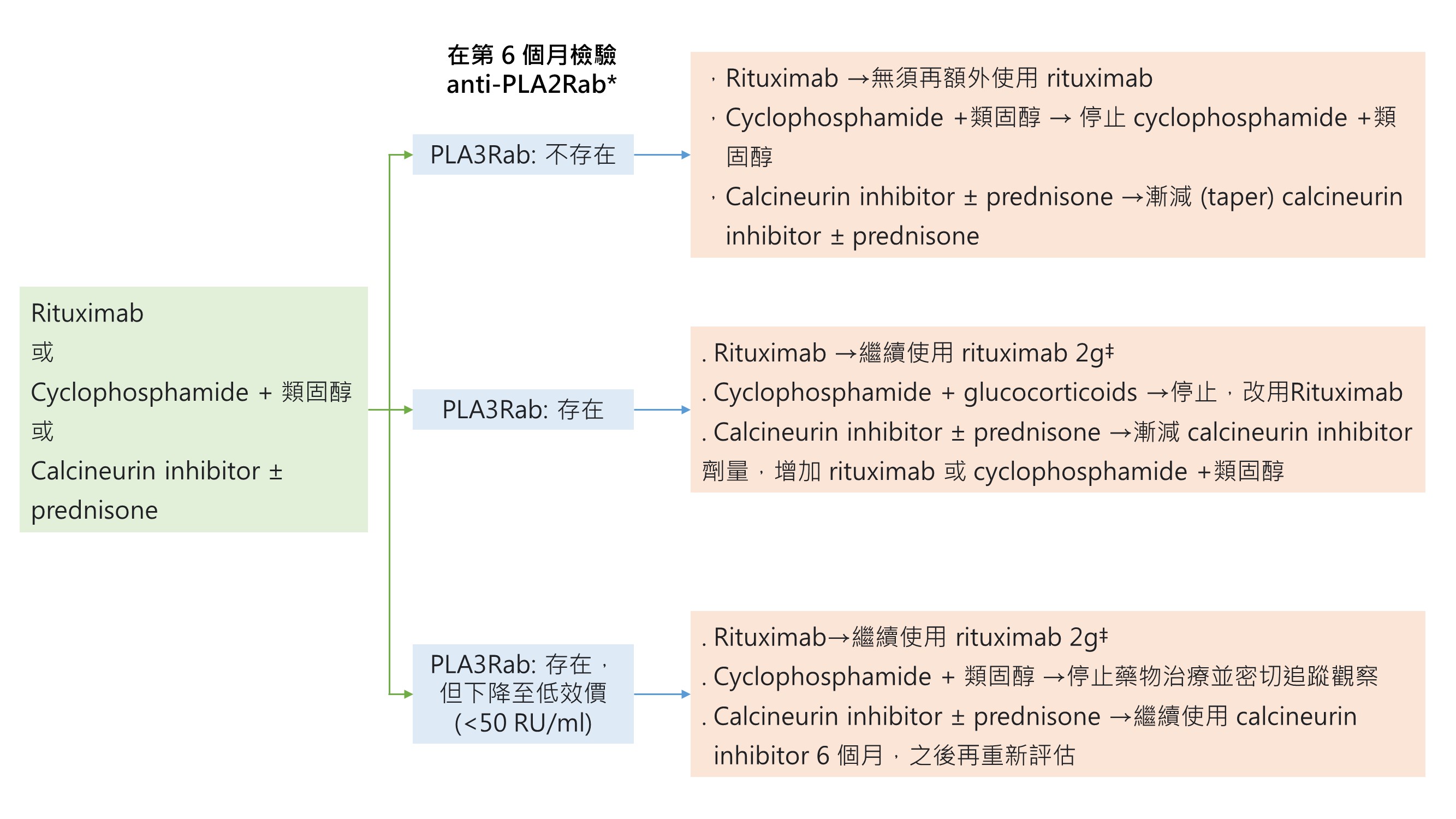
註 : 考慮致癌的風險,Cyclophosphamide 累積劑量不應超過 36g,為了保持安全,我們通常會限制在 25g ( 在 80 公斤的男性:週期性使用 6 個月 cyclophosphamide 2.5mg/Kg/day 等於 18g,6 個月連續性每天 1.5mg/Hg/day 等於 22 g)。
♣ 想懷孕的病人要使用低一點的計量 ( 最高 10g )
♣ CNI很難在後期達到免疫緩解 (late immunologic remission) ,在anti-PLA2R 抗體持續表現的病人,可考慮併用 rituximab。
♣ B細胞耗竭 (depletion) 不足用以評斷 rituximab 的療效,就算 B 細胞在周邊血液消失或很低,也要考慮額外的劑量。不過,在這些病人,建議照會專家中心。
♣ eGFR 應該穩定,若不是,則須要找出原因,如果eGFR下降是因為 MN的 活躍,就須要提供額外治療。
♣ 有些醫療中心會在第 3 個月就檢測 Anti-PLA2R 抗體,並調整治療。大部分的病人在治療 3 個月內就會有反應
† 免疫螢光法陰性代表免疫緩解,如果是使用ELISA檢測,2 RU/ml可以做為完全免疫緩解的閾值 (cutoff value)
‡ Rituximab 再次治療 ( retreatment) 須和初始治療方法相同,以 1g rituximab 注射1 到 2 次,間隔 2 周
3.4 特殊情形
治療要點 3.4.1:MN 病人治療後第一次復發的治療流程 (Fig 34)
Fig 34 : MN治療後第一次復發之處置
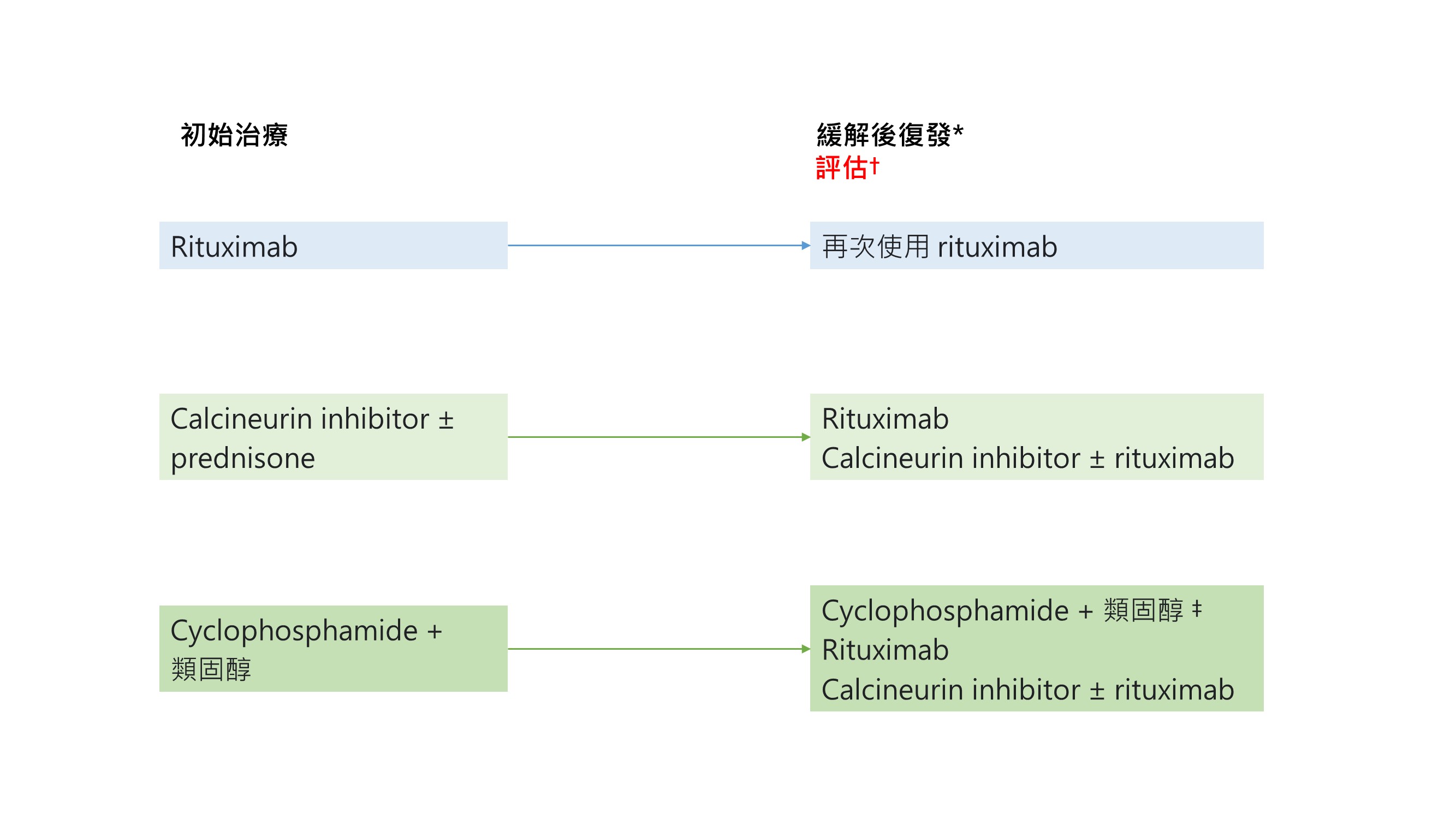
♣ 詳細的治療處方請見 Fig 32
♣ 復發的定義各異。有些作者定義復發為在完全或部分緩解後出現蛋白尿 >3.5g/d。我們建議將血清白蛋白和尿液 PCR ( P/C ratio ) 作為評估。如果 PCR 下降至 2~3.5g/d 但是血清白蛋白未上升至正常值,再來的 PCR 值上升應被視為治療抗性疾病而非緩解後的復發。對於部分緩解病患 (特徵是血清白蛋白恢復正常),復發的定義為蛋白尿上升同時血清白蛋白下降。
†免疫監測在這些狀況特別有價值,如果,在”臨床緩解”期間 anti-PLA2R抗體仍是陽性,這就是治療頑抗性疾病的證據。因此,對於 anti-PLA2R抗體陽性的病人,建議在緩解和復發時進行 anti-PLA2R 抗體檢驗。Anti-PLA2R抗體的病程應先發生於臨床病程。對於非常早期就復發的病人,檢討先前治療會失敗的原因很重要 (如., 用藥順從性,藥物濃度不夠,B細胞耗竭不足,出現 anti-rituximab 抗體)
‡ 雖然 cyclophosphamide 可以重複使用,但是,醫師要考慮到最高容忍劑量:如果需要保留生育力,累積劑量不應超過 10g;累積劑量不應超過 36g 以避免致癌的風險
治療要點 3.4.2 : 治療抗性 MN 病人的處置流程 (Fig 35)
Fig 35:MN 抗性疾病的處理
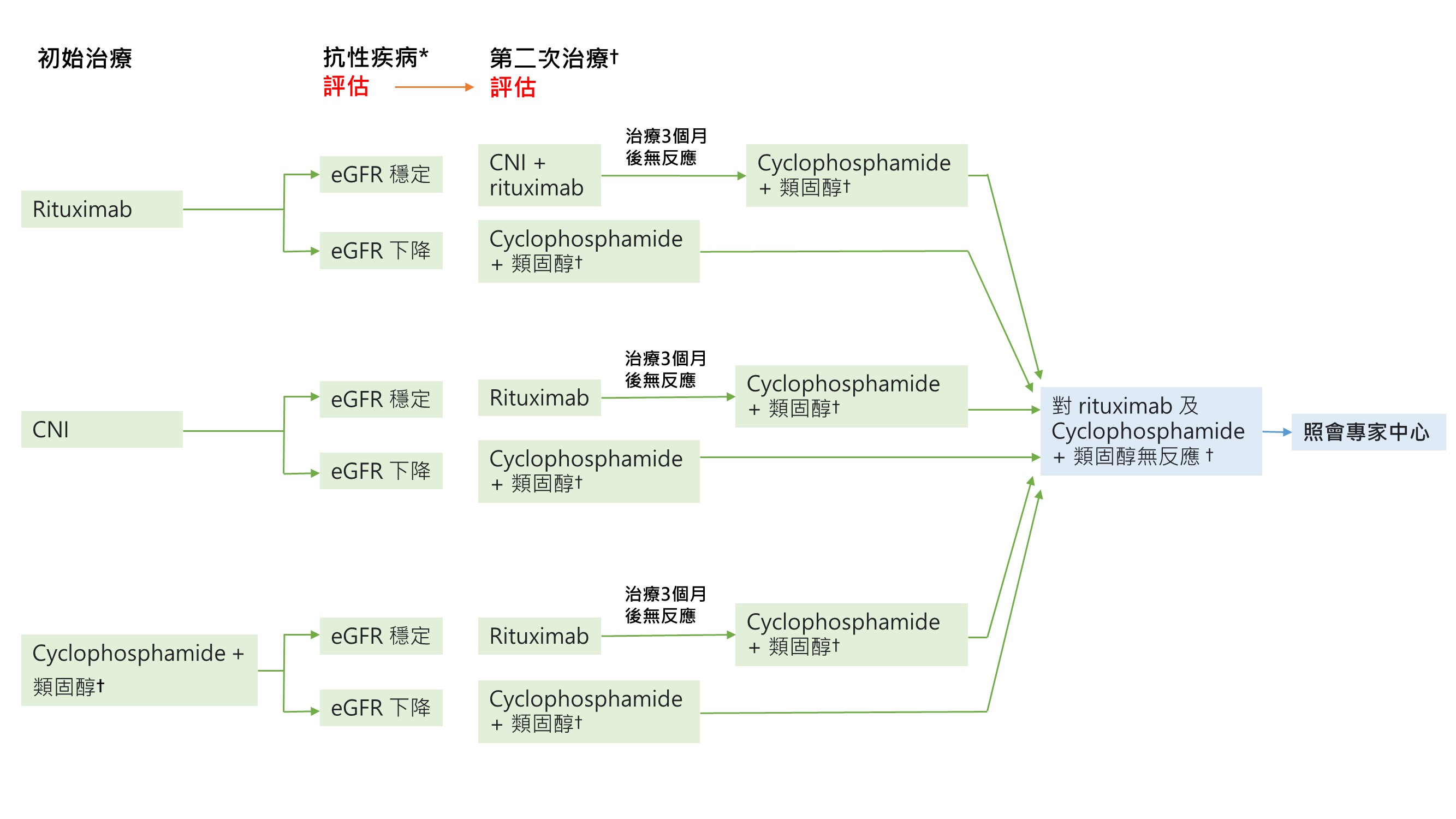
♣ 詳細的治療處方請見 Fig 32
* 評估:對於抗性疾病的病人,應對評估用藥順從性並監測藥物效果 ( 如., B細胞反應,anti-rituximab抗體,IgG濃度,cyclophosphamide治療時白血球減少症 [leukopenia],CNI藥物濃度)。持續性的蛋白尿並不足以定義為治療抗性。如果蛋白尿持續,而血清白蛋白上升,則應考慮續發性局部節段性腎絲球硬化症 (FSGS)。這可以從 anti-PLA2R 抗體陰性去支持。對於有持續蛋白尿但白蛋白在正常或接近正常、或是有持續蛋白尿但 anti-PLA2R 抗體陰性的病患,可以考慮做腎臟切片來確認活躍性MN的存在。
† 第二次治療的選擇取決於eGFR惡化程度。如果選擇rituximab做為二次治療,在3個月後零評估蛋白尿以及anti-PLA2R抗體的反應。Cyclophosphamide 必須考慮到大容忍劑量,如果需要保留生育力,累積劑量不應超過 10g;累積劑量不應超過36g 以避免致癌的風險。專家中心 ( expert center) 評估風險及益處,有可能會再使用更多
‡ 對 rituximab 或 cyclophosphamide 治療沒有反應的病人,應會診專家中心。這些中心可能會選擇實驗藥物 (bortezomib、anti-CD38、及belimumab) ,或是使用更高劑量的傳統免疫抑制治療。
♦ 目前仍未有可接受的MN抗性疾病的定義。
♦ 對於一開始接受治療時就有可測得 anti-PLA2R抗體的 MN 病患,抗性疾病可以定義為在使用第一線免疫抑制治療後 (有足夠的劑量和治療期間),仍有高或不變效價的 anti-PLA2R抗體。
♦ 持續性中等程度之蛋白尿不應用於定義抗性疾病,因為蛋白尿可在開始治療後仍持續 12~24 個月。
♦ 雖然持續 anti-PLA2R 抗體陽性代表治療抗性,有的病人會在達到蛋白尿部分緩解時仍有持續性低效價的 anti-PLA2R 抗體。這些病患必須密切追蹤、而免疫抑制治療常可以暫停。
♦ 很明顯地,在 anti-PLA2R 抗體陰性的病人去定義抗性疾病更為困難。
♦ 如果病人有持續性腎病症候群 (因此也有低血清白蛋白) 可以當作是抗性疾病 (如果期間大於 6 個月)。
♦ 在有低度蛋白尿和正常血清白蛋白的病人,持續性蛋白尿可能由續發性局部節段性腎絲球硬化症 (FSGS) 或其他因素來解釋 。
♦ 對於有持續性蛋白尿,但是血清白蛋白雖有上升但仍是減少的病人,可能很難去評斷。 這種狀況下,腎臟切片顯示小型緻密沉積 ( small dense deposits) 可用來定義持續疾病的活躍性。
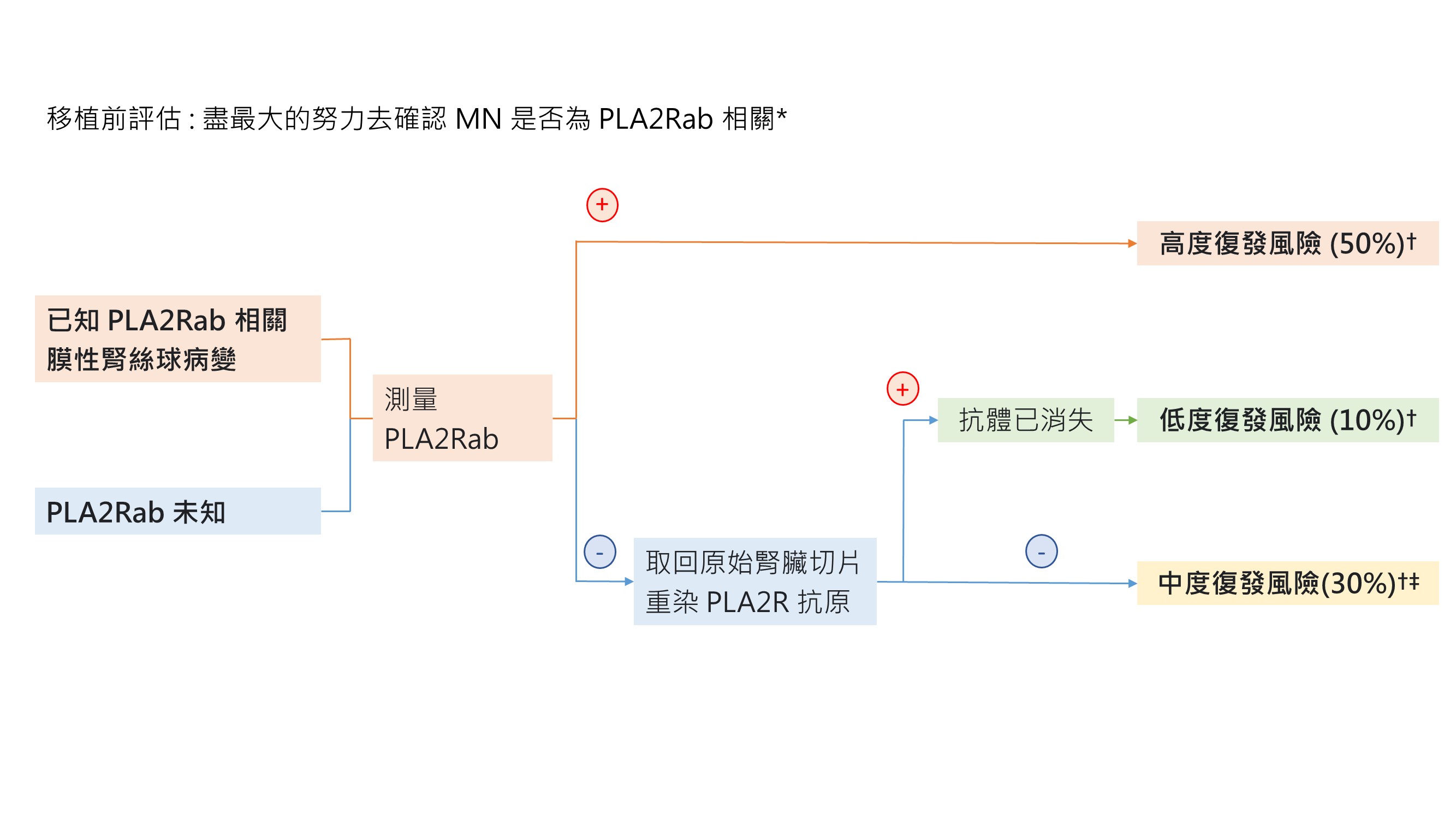
治療要點 3.4.3 : 評估接受腎臟移植之MN病人 ( Fig 36)
Fig 36 : 評估接受腎臟移植之MN病人

* 雖然資料有限,但是相同的治療流程應可適用於 anti-THSD7A 相關之 MN
† 臨床復發
這些是未定義抗原的 MN 病人預估之平均復發機率。我們建議這些病人的復發率以 THSD7A 抗原/抗體來評估可做較佳預測。
移植前期 ( pre-transplant) 評估
♦ 確認病患之 MN 是否和 anti-PLA2R抗體有關很重要。不論是舊有或是新的血清中 anti-PLA2R抗體陽性,或是腎臟切片有發現 PLA2R抗原,皆可確認為 anti-PLA2R 相關 MN。
♦ Anti-PLA2R 相關 MN 的病患在移植時,如果血清抗體陰性,可預測有較低復發風險。
♦ 相反的,如果 anti-PLA2R抗體陽性,則復發風險較高。
♦ 雖然研究指出高效價的 anti-PLA2R抗體 ( >45RU/ml ) 和風險增加有關,目前無足夠資料去定義一項閾值 (cutoff value)。
♦ 雖然缺乏 anti-THSD7A和腎臟移植的資料,但是相同的流程應該適用於評估 anti-THSD7A 相關 MN。
移植週術期和移植後期 ( peri- and post-transplant) 評估
♦ 目前沒有足夠資料去支持例行性腎臟切片或是先行使用 rituximab 治療,除非病患有多次復發病史和抗體陽性。
♦ 對於非 anti-PLA2R抗體相關之 MN 病患,蛋白尿必須在移植後持續每月監控至少 6~12 個月。如果蛋白尿 > 1g/d 則需執行腎臟切片。
♦ 對於 anti-PLA2R抗體相關之 MN 病患,建議移植後 6~12 個月內需要定期追蹤anti-PLA2R 抗體。追蹤頻率從移植前抗體效價高的病人 1 個月 1 次,到移植前測量不到抗體的病人 3 個月 1 次不等 ( 抗體在這些病人可再出現,代表疾病的再活化)。
♦ 若抗體效價持續高或是上升,皆可預期 MN 會復發,在這些病人,如果蛋白尿0.3~1.0g/d 時可以考慮腎臟切片。
♦ 復發的 MN 病人必須接受最大的保守、抗蛋白尿治療。如果蛋白尿 >1g/d,我們建議以 rituximab治療。
治療要點 3.4.4: 兒童 MN 處置之流程 (Fig 37)
Fig 37 : 兒童MN之處置

治療要點 3.4.5 : 在 MN 合併腎病症候群病人的預防性抗凝血治療,應基於血栓事件風險以及出血併發症風險的評估 (Fig 38)
♦ 腎病症候群會增加動脈及靜脈血栓風險,MN的病人有最大的風險。
♦ 血栓風險在疾病開始的前 6~12 個月特別高,因此在診斷時討論是否需要用抗凝血治療很重要。
Fig 38 : MN 病人的抗凝血治療
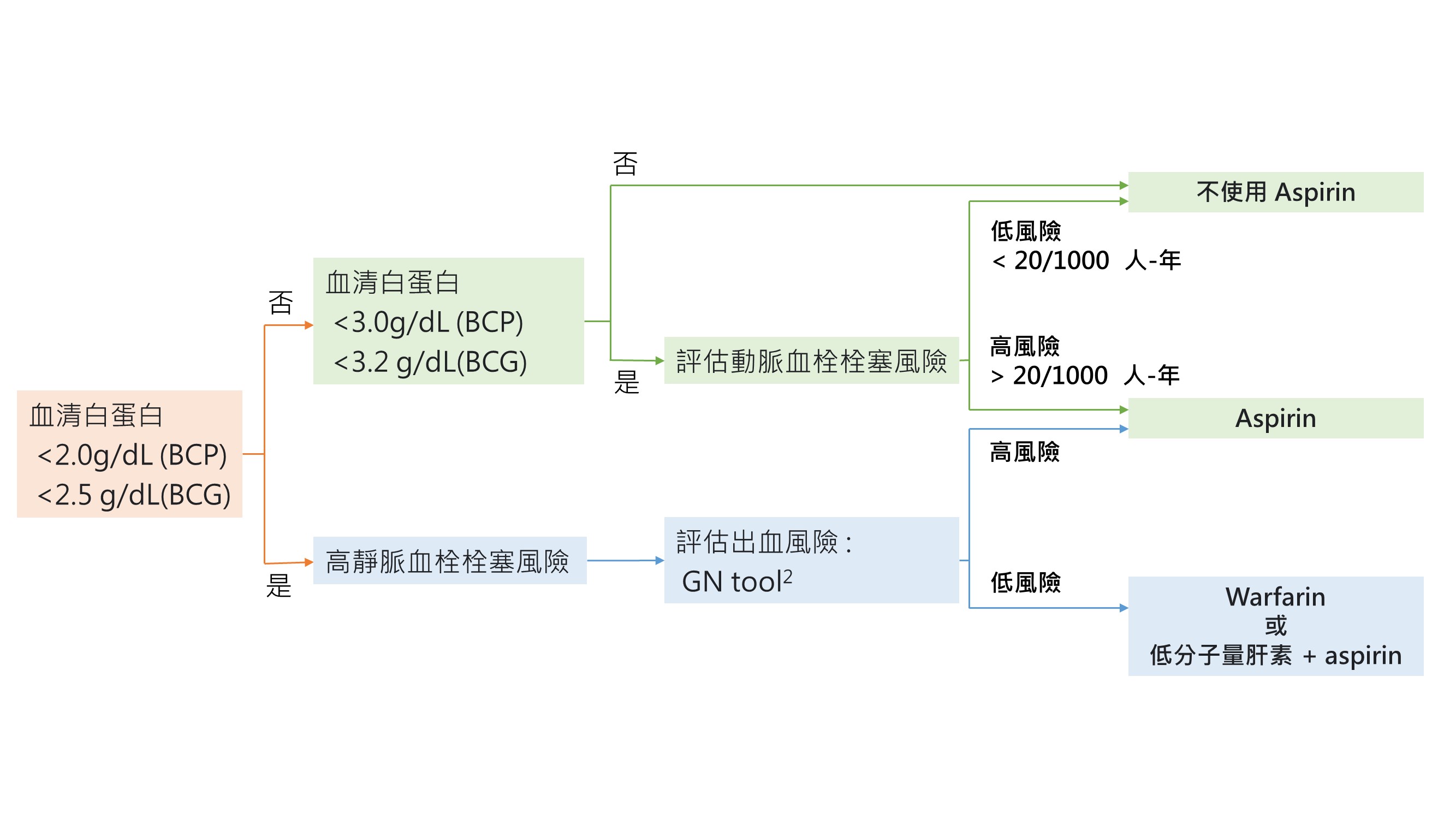
♣ 推薦的閾值是基於專家意見。當使用抗凝血治療,必須要衡量利與弊。以下為重要考量 :
- 血栓事件的風險和血清白蛋白濃度有關。必須知道血清白蛋白測量方法有很大不同,以 BCG 測量的血清白蛋白 2.5g/dl 等同於用 BCP 或 免疫散射法 (Immunonephelometry assay) 測量的2.0g/dl。大部分研究可能是用 BCG 方法。考量閾值時,BCG 法設在 2.5g/dl,BCP 或免疫散射法設在 2.0g/dl。
- 評估靜脈血栓風險和出血風險 (可參考此網頁上的計算: https://www.med.unc.edu/gntools/bleedrisk.html)
- MN合併腎病症候群病人也有動脈血栓風險。動脈血栓栓塞風險取決於年紀,過去動脈血栓病史,糖尿病,eGFR,抽菸,及腎病症候群嚴重程度。風險評估可用Framingham risk score去計算 ( 加上先前事件和蛋白尿 )
- 使用aspirin不足以預防靜脈血栓栓塞 (VTE);使用warfarin足以預防動脈血栓
- 使用warfarin治療: 在腎病症候群以及低eGFR病人上INR變化較大,在開始使用高劑量warfarin後會立即增加血栓風險。可以考慮先用低劑量低分子量肝素 (low-molecular-weight heparin),後續加入warfarin,達到治療效果後再停用heparin。另一種不錯的替代選擇是先使用低劑量低分子量肝素加aspirin 3個月,之後再轉換成warfarin,這樣可以依照蛋白尿程度去做調整
- 類固醇增加血栓風險;因此,在病患開始使用prednisone時不可以省略抗凝血治療
- 動脈血栓風險以Framingham risk score評估,低eGFR和嚴重蛋白尿會額外增加風險。 Framingham risk score所考量包含年紀、抽菸、血液膽固醇濃度、血壓
研究的建議 (Research recommendations)
診斷
- 評估anti-PLA2R抗體和anti-THSD7A抗體在診斷MN的準確度;在疾病出現臨床症狀前多久血清即呈現陽性?
- 比較評估anti-PLA2R抗體相關MN不同的技術,和評估診斷MN的準確性及適合的閾值
- 在大約20% anti-PLA2R和anti-THSD7A抗體皆為陰性的病人應用新技術 (laser capture microdissection followed by peptide digestion and mass spectrometry) 去分析額外的抗原,像是近期發現的exostosin 1/2, NELL-1, semaphorin 3B
預後
- 評估anti-PLA2R抗體效價對於預後的預測準確程度,考慮未接受治療 (自發性緩解) 和接受不同免疫抑制藥物的預後。決定適當的閾值。
- 評估anti-PLA2R抗體濃度在3~6個月期間的變化是否有預測預後的價值,無論病患是否有接受免疫抑制療法。找出最準確的閾值
- 評估anti-THSD7A抗體濃度從基礎值到追蹤期的變化,是否能提供準確預測預後的價值,考慮未接受治療 (自發性緩解) 和接受不同免疫抑制藥物的預後。決定適當的閾值
- 發展出能合併所有風險生物指標的計算方式去評估疾病惡化風險
- 了解表位擴張(epitope spreading)機轉及免疫優勢 (immunodominance),以及分析抗原決定區的活躍度 (epitope reactivity) 是否比PLA2R抗體效價還更有疾病預測價值
- 建立一個移植後評估復發的基因以及臨床風險指數
- 評估新發現的抗原所扮演的角色,以及它們和續發性病因的相關性
治療
- 我們應該將目標放在完全免疫緩解,還是 anti-PLA2R 抗體效價下降到某種程度就已足夠 ?
- 評估 CNI 在低惡化風險的 MN 病人,減少腎病症候群病程的效用
- 評估在高風險病患以 CNI 為基礎的藥物合用 (包含 rituximab ) 效用;我們應該循序合併使用免疫抑制劑嗎 ?
- 評估 rituximab 最佳的劑量/使用方法,以及 anti-rituximab 抗體對臨床的影響
- 在非常高風險的 MN 病人,比較以 rituximab 為基礎和以 cyclophosphamide 為基礎的治療效益
- 對標準免疫抑制治療無效的MN病人,評估使用新發展針對B 細胞 ( anti-CD20抗體,anti-BLyS/BAFF/APRIL抗體) 或針對漿細胞 ( plasma cell ) 治療 ( proteasome inhibitor 或 anti-CD38 抗體) 的效益
- 評估用抗原導向的標靶治療其潛力和可行性
特殊情形
- 評估適合的預防性抗凝血治療
- 評估測量 B 細胞 (包括記憶 B 細胞) 和 T 細胞的基因型對於預測疾病結果和對治療反應是否實用